淺談教材演示實(shí)驗(yàn)設(shè)計(jì)方案的改進(jìn)
許 智
(全日制普通高級(jí)中學(xué)教科書(必修加選修)《化學(xué)》第三冊第六單元第二節(jié)性質(zhì)實(shí)驗(yàn)方案設(shè)計(jì),“如圖1所示,給試管中的乙二酸晶體(H2C2O4?2H2O)加熱,將分解產(chǎn)物先通入干燥的?冷的小燒杯中,然后再通入澄清的石灰水中,觀察現(xiàn)象”?
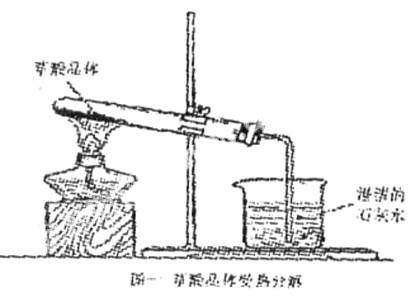
但在方案設(shè)施過程中,存在如下弊端:①試管口向下傾斜,乙二酸晶體熔化成液體,順試管壁流向試管口,導(dǎo)致實(shí)驗(yàn)不能成功;②將分解產(chǎn)物通入干燥的?冷的小燒杯中,檢驗(yàn)出來的水可能是乙二酸晶體分解出來的結(jié)晶水,不能證明乙二酸分解了;③乙二酸受熱揮發(fā)出蒸氣通入澄清的石灰水中,生成的CaC2O4是白色沉淀,對(duì)驗(yàn)證CO2有干擾,無法確證已乙二酸分解;④乙二酸加熱分解的產(chǎn)物可能為CO2?CO?H2O,其中CO是有毒氣體,必須處理掉等?
針對(duì)以上情況,某研究性學(xué)習(xí)小組進(jìn)行探究,設(shè)計(jì)出如下實(shí)驗(yàn)驗(yàn)證乙二酸的分解并測定其分解率,操作步驟如下:
①把乙二酸晶體放在烘箱中進(jìn)行烘烤,去掉結(jié)晶水,備用?
②按圖2連接好裝置?
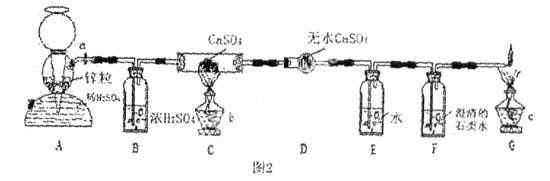
③檢查裝置的氣密性?
④打開活塞a,通入H2一會(huì)兒,再關(guān)閉a;點(diǎn)然酒精燈b?c?
⑤當(dāng)C裝置中固體消失后,停止加熱
⑥打開活塞a,繼續(xù)通入H2,直至冷卻?
試回答下列問題:
⑴裝置B的作用________;裝置E的作用_________?
⑵檢驗(yàn)該套裝置的氣密性的方法是__________________ ?
⑶若移取裝置A?B,會(huì)使所測的乙二酸的分解率_________(填“增大”?“減小”或“不變”)?
⑷可以代替裝置G的方法是_____________________?
⑸若稱取H2C2O4(烘干)的質(zhì)量為4.5g,實(shí)驗(yàn)結(jié)束后,稱得D?E?F分別增重0.95g?0.40g?1.98g,則乙二酸的分解率為_______________?
【解答導(dǎo)引】
⑴因從啟普發(fā)生器制得的氫氣中含有水蒸氣,必須除去;乙二酸為有機(jī)物,加熱會(huì)揮發(fā)出少量蒸氣,應(yīng)該通入水中加以溶解,以避免對(duì)后續(xù)實(shí)驗(yàn)產(chǎn)生干擾?
⑵因該套裝置使用的儀器較多,且多處有導(dǎo)管通入液體中,可打開啟普發(fā)生器的活塞a,產(chǎn)生氫氣,通過B?E?F瓶有無氣泡產(chǎn)生,可檢驗(yàn)其氣密性?
⑶因通入H2的目的是使乙二酸分解產(chǎn)生的氣體全部通入D?E?F裝置,避免少量分解產(chǎn)生的氣體滯留于裝置C中?不用裝置A?B,則D?E?F裝置增加的質(zhì)量將減小,所得到的分解率減少?
⑷因最后所得的氣體為CO,有毒不能排入大氣中,除點(diǎn)燃法外,可以用氣囊(或球)收集起來?
⑸因H2C2O4加熱→CO2↑+CO↑+H2O↑,因F增重1.98g,即生成的CO2質(zhì)量為1.98g,可得出分解的H2C2O4為4.05g,故乙二酸的分解率為90%?解題過程中,不能采用D?E裝置的增重?cái)?shù)據(jù),因部分未分解的乙二酸已在D裝置中冷卻,也就是說0.95g并不全是生成水的質(zhì)量,0.40g并不是全部未分解的乙二酸的質(zhì)量?可見此題隱含著數(shù)據(jù)干擾,若不善于挖掘隱含條件,此題極易致錯(cuò)?
【答案】
⑴干燥H2(或除去氫氣中混有的水蒸氣);溶解揮發(fā)出的乙二酸蒸氣,避免干擾實(shí)驗(yàn)?⑵打開啟普發(fā)生器的活塞a,觀察B?E?F瓶中是否有氣泡產(chǎn)生,若有氣泡產(chǎn)生,說明不漏氣,氣密性良好?⑶減小?⑷能氣囊(或球)收集起來?⑸90%?
收稿日期:2009-03-26

